Кадры и не только: ещё раз о лицензионных требованиях
Кадры и не только: ещё раз о лицензионных требованиях
Лицензирование сопровождает аптечные предприятия во многих ситуациях: добавление нового вида деятельности, смена адресов, превращение независимой аптеки в малую сеть… Неизменным спутником фармации остаётся и контроль соблюдения лицензионных требований, обязательных в повседневном труде фармацевта и провизора. В помощь специалистам 14 октября 2025 г. на платформе КС был проведён вебинар «Лицензионные требования к аптекам. Документы. Экспертиза». Ведущий фармацевтический инспектор Ассоциации аптечных учреждений (СРО) «СоюзФарма» Виктория Маховская подробно осветила данную тему, обратив внимание на целый ряд практических деталей. Представляем вниманию наших читателей детальный обзор второй части онлайн-лекции.
Не только на старте: когда лицензирование нужно… лицензиатам
Госуслугу по лицензированию фармдеятельности предоставляют центральный аппарат и территориальные органы Росздравнадзора (а иногда и региональные лицензирующие ведомства при подразделениях данной службы). Понадобиться она может не только соискателю.
Когда аптечное предприятие закрывается, действие лицензии на осуществление фармдеятельности должно быть прекращено. Это компетенция лицензирующего органа.
Бывает и так, что нужно внести изменения в реестр лицензий. Например, аптека больничная, она вправе вести только хранение и отпуск лекарств, а в ближайшее время к её функциям предстоит добавить ещё одну — розничную торговлю. Без уточнений в фармлицензии приступить к новым задачам нельзя!
Если в составе аптечной сети закрылись две или три аптеки — в реестр лицензий тоже необходимо внести коррективы. Как и в другой ситуации — при прекращении работы по одному из прежних направлений: когда производственная аптека становится аптекой готовых форм, это тоже должен утвердить лицензирующий орган.
Как оформляется запись в реестре
Красивых бланков лицензий, хорошо знакомых провизорам и фармацевтам с многолетним опытом, сегодня уже нет: в сфере фармдеятельности действует реестровая модель лицензирования. А значит, подтвердить право организации на работу могут другие формы документов: выписка из реестра, реестровая запись о предоставлении лицензии, уведомление.
Реестровая запись о выдаче лицензии формируется в ведомственной информационной системе Росздравнадзора, а затем идёт в единый реестр учёта лицензий для присвоения номера. Этот номер получает информационная система Службы.
Выписку из реестра аптека может скачать с сайта контролирующего органа: в документе будет указано, на какой день и время она действительна.
В квитанции госпошлины необходимости нет
На практике часто возникают вопросы о «технических моментах» подачи заявления на фармацевтическую лицензию. Первый из них — оплата госпошлины.
Здесь стоит отметить, что согласно п. 9 Постановления Правительства РФ от 12.03.2022 № 353 «Об особенностях разрешительной деятельности в Российской Федерации» за предоставление лицензии, внесение изменений в реестр лицензий и продление срока действия лицензии по заявлениям, поданным с 1 января 2024 г. по 31 декабря 2029 г., госпошлина не требуется.
От наименования до образования: что должен отметить в заявлении соискатель
Второй вопрос тоже вполне логичен: как правильно заполнить документ о выдаче, прекращении или уточнении фармлицензии?
Форма заявления — электронная. В неё предстоит внести несколько групп обязательных сведений. Среди них:
- организационно-правовая форма и полное наименование юрлица (ОГРН, ИНН);
- сокращённое наименование юрлица (если оно есть);
- адрес местонахождения юрлица, обязательно с индексом;
- для индивидуальных предпринимателей — фамилия, имя, отчество (если отчество есть), адрес места жительства и документ, удостоверяющий личность;
- контактный номер телефона (основной номер, номер ответственного сотрудника);
- адрес электронной почты (если есть);
- адреса мест ведения лицензируемого вида деятельности. Здесь понадобится указать, в том числе, кадастровый номер и тип объекта (организация оптовой торговли лекарственными средствами для медицинского применения / аптечная организация с указанием её вида);
- виды работ и услуг, которые планируется выполнять;
- сведения о сотрудниках (ФИО и СНИЛС);
- данные о наличии санитарно-эпидемиологического заключения о соответствии помещений требованиям санитарных правил — номер и дата выдачи. Они нужны всем соискателям фармлицензий, кроме медорганизаций и их обособленных подразделений;
- информация, подтверждающая наличие у соискателя (на праве собственности или на ином законном основании) необходимых для фармдеятельности производственного объекта или объектов и оборудования, соответствующих установленным требованиям. Данная графа обязательна для всех соискателей, которые не относятся к медорганизациям;
- сведения о профильном образовании сотрудников, высшем или среднем, а также о сертификатах или пройденной аккредитации понадобятся всем соискателям (кроме медорганизаций и их подразделений);
- медорганизациям будет нужна информация о наличии лицензии на меддеятельность;
- данные о пройденных сотрудниками курсах ДПО по розничной торговле лекарственными препаратами и наличии права на ведение медицинской деятельности потребуются обособленным подразделениям медорганизаций.
Процедура получения лицензии
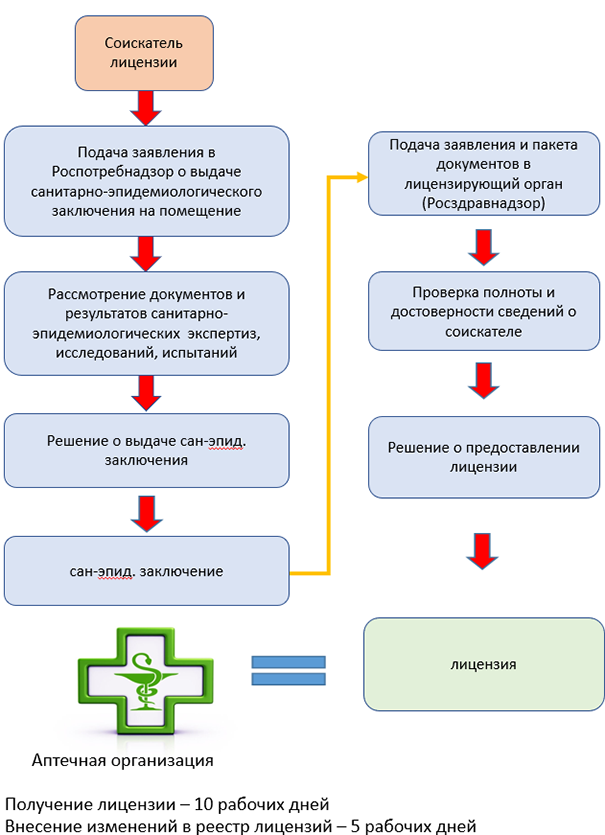
Семь раз отмерь: какие обстоятельства уточнит лицензирующий орган
Вся перечисленная информация необходима Росздравнадзору для проверки соответствия лицензионным требованиям. Контролирующий орган внимательно изучит её и направит межведомственные запросы, чтобы перепроверить некоторые факты. А именно:
- в Федеральной налоговой службе — сведения об ИНН налогоплательщика, ОГРН юрлица и ОГРН индивидуального предпринимателя;
- в Социальном фонде — данные о наличии у соискателя работников, которые заключили с ним трудовой договор и при этом заняты в сфере обращения лекарственных средств;
- в Росреестре — информацию о том, что соискатель (на праве собственности или на ином законном основании) располагает необходимыми для фармацевтической деятельности помещениями, зданиями или сооружениями;
- в Рособрнадзоре — факт наличия у сотрудников профильного образования (фармацевтического или ветеринарного), а также сертификата специалиста или пройденной аккредитации;
- в Роспотребнадзоре — подтверждение выдачи санэпидзаключения о соответствии помещений требованиям санитарных правил для фармдеятельности в сфере обращения лекарственных средств.
Если эти сведения найти затруднительно, заявитель может представить документы (копию диплома и т. д.) по своей инициативе.
Время ожидания: сроки зависят от задачи
Заявление на получение фармлицензии обрабатывается не дольше 10 рабочих дней с даты его регистрации на портале Госуслуг. Если речь идёт о закрытых административно-территориальных образованиях (ЗАТО), период будет другим — не более 20 рабочих дней.
Заявление о внесении изменений в реестр лицензий на ведение фармдеятельности (перед началом выполнения новых задач или при изменении адреса) рассматривается до пяти рабочих дней. Для ЗАТО срок тот же — 20 дней.
Если лицензиат просит уточнить данные в реестре из‑за необходимости закрыть одну или несколько аптек или отказаться от одного из видов работ, составляющих фармдеятельность (например, изготовления лекарственных препаратов), ответ на заявление будет дан максимум за три рабочих дня. Тот же срок предоставления госуслуги определён для прекращения действия фармлицензии.
Рубикон перейдён: что включает в себя лицензионный контроль?
Подробно рассказав о требованиях к соискателям и государственной услуге по лицензированию фармдеятельности, лектор обратила внимание слушателей на ситуации, когда оптовое предприятие, сельское медучреждение, аптека или аптечная сеть уже получили разрешение на фармацевтическую деятельность. Теперь они не соискатели, а лицензиаты, и соответствие их работы лицензионным нормам будет проверяться регулярно: лекарства — это то, что тесно связано с жизнью и здоровьем.
Как и соискателю, лицензиату нужно располагать производственными объектами и оборудованием по месту ведения фармдеятельности. Эти здания, помещения, сооружения и аппаратура должны отвечать действующим нормам. А именно:
- у оптовых предприятий — требованиям статьи 54 ФЗ «Об обращении лекарственных средств», у аптек — положениям статьи указанного закона;
- у оптовых фармкомпаний — Правилам надлежащей дистрибьюторской практики в рамках ЕАЭС (утв. Решением Совета ЕЭК от 03.11.2016 № 80);
- у всех без исключения лицензиатов — Правилам хранения лекарственных средств (утв. Приказом Минздрава России от 29.04.2025 № 260н);
- у аптек — Правилам надлежащей аптечной практики (утв. Приказом Минздрава России от 29.04.2025 № 259н).
Для медорганизаций-лицензиатов главное условие — наличие разрешения на ведение основной, медицинской деятельности.
Буква закона: надлежащая практика и не только
Следующая задача лицензиата — знание и соблюдение действующих норм права. Значительная часть лицензионных требований к фармдеятельности сосредоточена в подзаконных актах, утверждённых приказами Минздрава. Некоторые правила утверждены законами или наднациональными юридическими документами — так обстоят дела, например, в дистрибьюторском звене.
Для оптовой фармкомпании лицензионными нормами являются:
- статьи 53, 54 и часть седьмая статьи 67 ФЗ «Об обращении лекарственных средств»;
- статья названного закона — а именно запрет на реализацию поддельных, контрафактных и бракованных препаратов;
- Правила надлежащей дистрибьюторской практики в рамках ЕАЭС;
- Правила хранения лекарственных средств;
- правила регистрации операций, связанных с обращением препаратов предметно-количественного учёта, и правила ведения и хранения специальных журналов учёта таких операций (утв. Приказом Минздрава России от 17.06.2013 г. № 378н).
Для аптеки или аптечной сети список нормативных актов с лицензионными требованиями несколько иной:
- Правила надлежащей аптечной практики;
- Правила хранения лекарственных средств;
- Правила отпуска лекарственных препаратов (утв. Приказом Минздрава от 07.03.2025 № 100н);
- Правила отпуска наркотических средств и психотропных веществ, зарегистрированных в качестве лекарственных препаратов (утв. Приказом Минздрава от 07.03.2025 № 100н), если аптечная организация работает с такой продукцией;
- Правила регистрации операций, связанных с обращением препаратов ПКУ, и правила ведения и хранения специальных журналов учёта этих операций;
- часть шестая статьи 55, статья и часть седьмая статьи 67 ФЗ «Об обращении лекарственных средств».
Для тех медорганизаций, которые ведут фармдеятельность, лицензионными нормами будут правила отпуска лекарственных препаратов и положения части седьмой статьи 67 ФЗ «Об обращении лекарственных средств».
Когда «обязательный минимум» не обязателен
Возникает вопрос: для каждой ли аптеки необходим минимальный ассортимент (ведь он предусмотрен частью шестой статьи 55 ФЗ «Об обращении лекарственных средств»)? Всё зависит от тех видов деятельности, которые предусмотрены в фармацевтической лицензии.
Если аптека больничная и в выписке из реестра лицензий не отмечено право вести розничную торговлю, минимальный ассортимент с неё требовать нельзя! Как и с производственной аптеки, которая отпускает только экстемпоральные препараты, но не работает с готовыми формами.
Взаимодействие с маркировкой: основные принципы
Отдельно стоит сказать о работе с системой МДЛП — она является лицензионным требованием к фармдеятельности в силу статьи 67 ФЗ «Об обращении лекарственных средств». Передавать в эту систему данные о движении лекарственных препаратов обязательно на всех этапах: от производства до реализации или утилизации.
А согласно ФЗ «О применении контрольно-кассовой техники при осуществлении расчётов в РФ» те пользователи, которые ведут расчёты за маркированную продукцию, обязаны формировать данные в виде запросов о коде маркировки и уведомлений о реализации маркированного товара в электронной форме с применением подходящей для этих задач ККТ. Кассовая аппаратура передаёт информацию оператору маркировки через оператора фискальных данных.
Напомним о некоторых организационных моментах передачи аптекой (или медорганизацией) данных в систему МДЛП.
Участник обращения лекарственных препаратов, который вывел их из оборота, в течение пяти рабочих дней со дня реализации/отпуска/передачи лекарств в отделение передаёт сведения в систему маркировки. При розничной продаже лекарств аптека выполняет эту задачу с применением контрольно-кассовой техники. При льготном отпуске — с помощью регистраторов выбытия. Регистраторы выбытия понадобятся и больничным аптекам, которые выдают препараты в отделения медорганизации по их требованиям.
Утилизация просроченных и «некондиционных» препаратов тоже связана с маркировкой. В течение пяти рабочих дней с момента их передачи на уничтожение участник обращения лекарственных средств передаёт в систему мониторинга сведения по схеме 541. Как только был получен акт о проведении утилизации, у аптеки или другого субъекта есть пять рабочих дней, чтобы передать информацию о факте уничтожения по схеме .
За опоздание или ошибки при внесении данных в систему МДЛП предусмотрена ответственность по статье 6.34 КоАП. Для должностных лиц штраф составляет 5–10 тысяч рублей, для юридических — от 50 до 100 тысяч.
ЕГИСЗ: внесение данных — задача срочная
Следующий блок требований к организациям-лицензиатам касается кадрового вопроса. Часть норм хорошо знакома недавним соискателям:
- оптовое предприятие, аптека или аптечная сеть располагают коллективом дипломированных фармацевтов и провизоров с пройденной аккредитацией (либо сертификатами специалистов) и надлежащим образом оформленными трудовыми договорами;
- индивидуальный предприниматель, руководящий аптекой, сам должен быть провизором или фармацевтом с сертификатом либо аккредитацией;
- медицинские работники сельского ФАП или сельской больницы прошли курс ДПО по розничной торговле лекарственными препаратами.
Но как только соискатель стал лицензиатом, появляется ещё ряд обязанностей. И первая из них — размещение сведений о предприятии и сотрудниках в двух подсистемах ЕГИСЗ: Федеральном реестре медорганизаций (ФРМО) и Федеральном регистре медработников (ФРМР). Задача эта срочная: даже если лицензия была получена только вчера, приступить к внесению данных нужно немедленно.
ФРМО: отмечаем должности без единой ошибки
Начать нужно с Федерального реестра медорганизаций. В графу «Карточка организации» аптечное предприятие или ИП вносит сведения о видах деятельности и контактов. В следующем параграфе «Лицензирование» должна размещаться лицензия на фармдеятельность. Она загружается с сайта Росздравнадзора. Если этот документ не появился в личном кабинете аптечной организации в ФРМО, нужно сообщить об этом в территориальный орган РЗН.
Внимание: сами аптечные предприятия свои лицензии в ФРМО не загружают!
А вот в подразделе о планируемых лицензиях стоит написать о намеченном открытии новой аптеки в составе предприятия.
Раздел «Здания» включает в себя основную информацию, адреса, сведения о праве собственности, этажи и помещения, а также дополнительные данные. Аналогично заполняется и графа «Структурные подразделения»: вначале основная информация, затем данные о зданиях и помещениях и дополнительные сведения.
Камнем преткновения для аптечных организаций зачастую становится глава ФРМО «Штатное расписание». Здесь предстоит добавить запись штатного расписания с указанием занятых штатных единиц, внешних совместительств и вакансий. В каждой «строке» вначале нужно отметить фамилию, имя и отчество сотрудника. Назвать должность — второй шаг, возможный только после того, как человека «представили» электронной системе.
Задача достаточно непроста: должность предстоит отметить без единой ошибки, в полном соответствии с номенклатурой, определённой Приказом Минздрава от 02.05.2023 № 205н. Малейшая неточность, увы, может стать основанием для отказа в периодической аккредитации провизора или фармацевта.
После «Штатного расписания» лицензиата ждёт параграф «Оборудование». Здесь уже немногим легче: детальный список видов оборудования приведён в пункте 11 Правил хранения лекарственных средств. Остаётся заполнить подпараграфы об основной информации, моделях и производителях приборов, дополнительных сведениях, местоположении и количестве.
Правда, без нестандартных ситуаций не обходится и здесь: как сообщили фарминспектору слушатели вебинары, некоторые областные минздравы требуют внести в названный раздел сведения о находящихся в аптеке… электрочайниках.
ФРМР: информация об отпусках и квалификационных категориях
После внесения данных в ФРМО предстоит перейти к Федеральному регистру медработников. Заполнение этого регистра тоже требует огромного внимания к деталям: как и в случае с графой ФРМО «Штатное расписание», любая неточность грозит вероятным отказом в периодической аккредитации специалиста.
В параграф «Карточка сотрудника» вносится ФИО, информация о документах и основных сведениях — гражданстве, СНИЛС и нескольких других параметрах.
В разделе «Документы» должны быть паспортные данные.
Глава «Личное дело» будет более подробной. В ней указывают не только место работы, структурное подразделение и реквизиты трудового договора, но и информацию о временном отсутствии сотрудника в организации. Если фармацевт или провизор находится в отпуске, на больничном или в декрете, это тоже нужно отразить в ФРМР.
В части «Адреса» аптечное предприятие отмечает место постоянной регистрации и фактического проживания своих сотрудников.
Особое внимание стоит обратить также на раздел «Образование». Здесь должны быть указаны сведения о среднем общем, профессиональном и послевузовском образовании, информация о пройденных программах ДПО, реквизиты сертификата специалиста, данные об аккредитации и квалификационная категория.
В дальнейшем посетить ФРМР понадобится сотрудникам организации — ведь через этот информационный ресурс подают документы на аккредитацию.
Аптечный самоконтроль: опираемся на чек-листы
Проверять себя на соответствие лицензионным требованиям аптека может в процессе внутреннего аудита: такой контроль, по новым Правилам НАП, обязательно проводить не реже чем раз в полгода.
В качестве «стандарта» подойдут «памятки» Росздравнадзора, утверждённые пока ещё действующими, но планируемыми к обновлению документами:
- Приказом РЗН от 16 сентября 2022 года № 8700 «Об утверждении форм проверочных листов… в сфере обращения лекарственных средств»;
- Приказом РЗН от 26 августа 2022 г. № 7974 «Об утверждении форм оценочных листов…».
В этих листах есть ссылки на устаревшие нормативные документы (старые версии Правил НАП, Правил хранения и Правил отпуска), однако большинство ключевых принципов остаётся прежними.
От штрафа до «паузы»: ответственность за нарушения
Соблюдать лицензионные требования нужно неукоснительно, поскольку фармдеятельность — часть сферы охраны здоровья. В некоторых ситуациях даже недочёты могут быть признаны грубыми.
Грубое нарушение — это невыполнение лицензиатом хотя бы одной из лицензионных норм, если оно повлекло серьёзные последствия. Например:
- возник риск причинения вреда жизни и здоровью граждан, вреда животным, растениям, окружающей среде;
- есть человеческие жертвы или причинён тяжкий вред здоровью граждан;
- причинён вред средней тяжести здоровью двух и более граждан или вред животным, растениям, окружающей среде.
Если было допущено нарушение лицензионных требований, но, к счастью, оно ещё не оказалось грубым, лицензиат несёт ответственность согласно части третьей статьи 14.1. Кодекса об административных правонарушениях. Для юридических лиц это штраф в размере от 30 до 40 тысяч рублей.
Грубые нарушения лицензионных норм подлежат ответственности уже по части четвёртой статьи 14.1. КоАП. Для индивидуальных предпринимателей это административный штраф в размере от 4 до 8 тысяч рублей, либо приостановление деятельности сроком до 90 суток. Для юрлиц сумма штрафа составит от ста до двухсот тысяч рублей — и тоже возможна «постановка на паузу».
За реализацию поддельных либо контрафактных лекарств и медизделий, а также фальсифицированных БАД санкции предусмотрены уже статьёй 6.33 КоАП:
- для должностных лиц — штраф от ста до шестисот тысяч рублей;
- для ИП — штраф в том же размере, либо приостановление фармдеятельности на период до 90 дней;
- для юрлиц — штраф от одного до пяти миллионов рублей, либо «постановка на паузу» на тот же срок.
Ещё для одного лицензионного требования — работы с системой МДЛП — наказание определено статьёй 6.34 названного кодекса (о ней говорилось выше).
Подводя итоги вебинара, фарминспектор рассказала о некоторых новых тенденциях в судебной практике по административным делам в отношении аптечных организаций: в 2025 году органы прокуратуры впервые стали проверять данные, внесённые аптеками в ФРМР и ФРМО.
Ошибки в заполнении карточек в этих подсистемах ЕГИСЗ нередко квалифицировались как грубое нарушение. Виновными в допущенных недочётах зачастую признавались предприятия, а не их руководители (т. е. юридические, а не должностные лица).
источник: www.katrenstyle.ru
